История создания периодической системы. История создания периодической системы Кто изобрел периодическую таблицу химических элементов
В своей работе 1668 года Роберт Бойль привёл список неразложимых химических элементов. Было их на тот момент всего пятнадцать. При этом учёный не утверждал, что кроме перечисленных им элементов больше не существует и вопрос об их количестве оставался открытым.
Через сто лет французский химик Антуан Лавуазье составил новый список из известных науке элементов. В его реестр попали 35 химических веществ, из которых 23 были впоследствии признаны теми самыми неразложимыми элементами.
Работа по поиску новых элементов велась химиками во всём мире и продвигалась вполне успешно. Решающую роль в этом вопросе сыграл русский учёный-химик Дмитрий Иванович Менделеев: именно ему пришла в голову идея о возможности существования взаимосвязи между атомной массой элементов и их местом в "иерархии". По его собственным словам "надо искать... соответствия между индивидуальными свойствами элементов и их атомными весами".
Сопоставляя между собой известные в то время химические элементы, Менделеев после колоссальной работы обнаружил в итоге ту зависимость, общую закономерную связь между отдельными элементами, в которой они предстают как единое целое, где свойства каждого элемента является не чем-то само собой существующим, а периодически и правильно повторяющимся явлением.
Так в феврале 1869 года был сформулирован периодический закон Менделеева . В том же году 6 марта доклад, подготовленный Д.И. Менделеевым, под названием "Соотношение свойств с атомным весом элементов" был представлен Н.А. Меншуткиным на заседании Русского химического общества.
В том же году публикация появилось в немецком журнале "Zeitschrift für Chemie", а в 1871 году в журнале "Annalen der Chemie" вышла развёрнутая публикация Д.И. Менделеева, посвящённая его открытию - "Die periodische Gesetzmässigkeit der Elemente" (Периодическая закономерность химических элементов).
Создание периодической таблицы
Несмотря на то, что идея сформировалась у Менделеева за довольно короткий срок, оформить свои умозаключения он долго не мог. Ему было важно представить свою идею в виде ясного обобщения, строгой и наглядной системы. Как сказал однажды сам Д.И. Менделеев в беседе с профессором А.А. Иностранцевым: "Все в голове сложилось, а выразить таблицей не могу".
По данным биографов, после этого разговора учёный работал над созданием таблицы три дня и три ночи, не ложась спать. Он перебирал различные варианты, в которых могли бы быть скомбинированы элементы для организации в таблицу. Осложнялась работа и тем, что на момент создания периодической системы далеко не все химические элементы были известны науке.
В 1869-1871 годах Менделеев продолжал развивать выдвинутые и принятые научным сообществом идеи периодичности. Одним из шагов было введение понятия о месте элемента в периодической системе как совокупности его свойств в сопоставлении со свойствами других элементов.
Именно на основе этого, а также с опорой на результаты, полученные в ходе изучения последовательности изменения стеклообразующих оксидов, Менделеев исправил значения атомных масс 9 элементов, в числе которых были бериллий, индий, уран и другие.
В ходе работы Д.И. Менделеев стремился заполнить пустые клетки составленной им таблицы. В результате в 1870 году им было предсказано открытие неизвестных на тот момент науке элементов. Менделеев вычислил атомные массы и описал свойства трёх ещё не открытых тогда элементов:
- "экаалюминия" - открыт в 1875 году, назван галлием,
- "экабора" - открыт в 1879 году, назван скандием,
- "экасилиция" - открыт в 1885 году, назван германием.
Следующие его реализовавшиеся прогнозы - открытие ещё восьми элементов, в том числе полония (открыт в 1898 году), астата (открыт в 1942-1943 годах), технеция (открыт в 1937 году), рения (открыт в 1925 году) и франция (открыт в 1939 году).
В 1900 году Дмитрий Иванович Менделеев и Уильям Рамзай пришли к выводу о необходимости включения в периодическую систему элементов особой, нулевой группы. Сегодня эти элементы называются благородными газами (до 1962 года эти газы называли инертными).

Принцип организации периодической системы
В своей таблице Д.И. Менделеев расположил химические элементы по рядам в порядке возрастания их массы, подобрав длину рядов таким образом, чтобы химические элементы в одной колонке имели похожие химические свойства.
Благородные газы - гелий, неон, аргон, криптон, ксенон и радон неохотно реагируют с другими элементами и проявляют низкую химическую активность и потому находятся в крайней правой колонке.
В противоположность этому элементы самой левой колонки - литий, натрий, калий и прочие реагируют с другими веществами бурно, процесс носит взрывной характер. Аналогично ведут себя элементы в других колонках таблицы - внутри колонки эти свойства подобны, но варьируются при переходе от одной колонки к другой.
Периодическая система в своем первом варианте просто отражала существующее в природе положение дел. Первоначально таблица никак не объясняла, почему это должно быть именно так. И только с появлением квантовой механики стал понятен истинный смысл расположения элементов в периодической таблице.
Химические элементы вплоть до урана (содержит 92 протона и 92 электрона) встречаются в природе. Начиная с номера 93 идут искусственные элементы, созданные в лабораторных условиях.
И как же запомнить все 118 элементов?
Это долгое время было сложным вопросом. Над проблемой, как упорядочить элементы, бились лучшие умы. У кого-то получалась стройная картинка, у других выходили винтовые лестницы и другие фигуры. Давно было замечено, что свойства элементов повторяются с ростом атомной массы, есть некая зависимость и цикличность. Один из ученых смог создать таблицу, но в качестве главного свойства взял валентность и при проверке все рассыпалось. А он так близко был к решению задачи.
Что такое «валентность»?
Свойство элементов вступать в связи, создавать вещества. Если просто, то со сколькими другими атомами этот элемент может образовывать соединения. В электронных облаках вокруг ядра есть области меньшей плотности, в эти дыры могут залетать электроны другого элемента. И тогда возникает связь между ними. От количества таких «пустых» областей зависит активность того или иного элемента. Но не забывайте, что в наших статьях мы стараемся все упрощать. Сейчас химики не любят слово валентность, но используя его легче запомнить сколько потенциальных связей может установить элемент.
И так, что там химик Менделеев?

Вообще, Дмитрий Иванович не был химиком в нашем понимании. Он был ученым, специалистом в разных областях, он придумал транспортировку нефти по трубопроводу. Считается, что он изобрел русскую водку. Это не совсем правда. Бухали и до него. Ему приписывается оптимальная крепость напитка в 40 градусов. Менделеев почти двадцать лет искал способ классификации элементов, раскладывая карточки с их именами то так, то эдак. Есть легенда, что таблица приснилась ему во сне. Когда десятки лет обдумываешь загадку, еще не то приснится.
И ему удалось все поставить на свои места?
И да и нет. Дело в том, что в 1869 году были известны только 63 элемента и в таблице оставались пустые места, а некоторые элементы не хотели вписываться в свои ячейки. Таблица получилась наглядной, учитывала множество характеристик, и доказала периодичность свойств элементов. Мало того, с развитием науки были обнаружены новые элементы. Они встали на места, зарезервированные ученым, и имели те свойства, которые он предсказал. А некоторым элементам Менделеев изменил ошибочные атомные массы, например урану. И оказался прав!
И как пользоваться такой таблицей?
Со времен Менделеева она претерпела изменения, но главная идея - периодичность свойств осталась неизменной. По вертикальным колонкам расположены группы элементов, которые обладают похожими свойствами, по горизонтали сами «периоды». От щелочных металлов до «благородных газов». Удивительно, но имеющие разные атомные массы элементы так похожи! Многие слышали о натрии и калии? Они образуют похожие соединения, их химические свойства почти одинаковы, несмотря на то, что их атомные массы различаются намного. Та же история и в правой таблице фтор и хлор однотипные газы.
Как он смог это установить?

Мы знаем, что свойства химического элемента полностью зависят от строения его атома, а 150 лет назад об этом не знали. Все это результат смекалки и десятилетий упорного труда.
Таблица какая-то рваная в ней есть дырки и отдельные блоки снизу.
В природе нет ничего идеального. Даже в нижних блоках есть своя периодичность, например уменьшение электронной оболочки и уровень ионизации. Лантаноиды и актиноиды вынесли в нижний ряд, чтобы сделать таблицу компактнее. Даже в том, что таблица становится шире есть своя периодичность, это повторяется и в соседнем ряду.
Периодический закон был открыт Д.И. Менделеевым в ходе работы над текстом учебника «Основы химии», когда он столкнулся с трудностями систематизации фактического материала. К середине февраля 1869 г., обдумывая структуру учебника, ученый постепенно пришел к выводу, что свойства простых веществ и атомные массы элементов связывает некая закономерность.
Открытие периодической таблицы элементов было совершено не случайно, это был результат огромного труда, длительной и кропотливой работы, которая была затрачена и самим Дмитрием Ивановичем, и множеством химиков из числа его предшественников и современников. «Когда я стал окончательно оформлять мою классификацию элементов, я написал на отдельных карточках каждый элемент и его соединения, и затем, расположив их в порядке групп и рядов, получил первую наглядную таблицу периодического закона. Но это был лишь заключительный аккорд, итог всего предыдущего труда…» - говорил ученый. Менделеев подчеркивал, что его открытие было итогом, завершившим собой двадцатилетнее размышление о связях между элементами, обдумывание со всех сторон взаимоотношений элементов.
17 февраля (1 марта) рукопись статьи, содержащая таблицу под названием «Опыт системы элементов, основанной на их атомном весе и химическом сходстве», была закончена и сдана в печать с пометками для наборщиков и с датой «17 февраля 1869 г.». Сообщение об открытии Менделеева было сделано редактором «Русского химического общества» профессором Н.А. Меншуткиным на заседании общества 22 февраля (6 марта) 1869 г. Сам Менделеев на заседании не присутствовал, так как в это время по заданию Вольного экономического общества обследовал сыроварни Тверской и Новгородской губерний.
В первом варианте системы элементы были расставлены ученым по девятнадцати горизонтальным рядам и по шести вертикальным столбцам. 17 февраля (1 марта) открытие периодического закона отнюдь не завершилось, а только началось. Его разработку и углубление Дмитрий Иванович продолжал еще в течение почти трех лет. В 1870 г. Менделеев в «Основах химии» опубликовал второй вариант системы («Естественную систему элементов»): горизонтальные столбцы элементов-аналогов превратились в восемь вертикально расположенных групп; шесть вертикальных столбцов первого варианта превратились в периоды, начинавшиеся щелочным металлом и заканчивающиеся галогеном. Каждый период был разбит на два ряда; элементы разных вошедших в группу рядов образовали подгруппы.
Сущность открытия Менделеева заключалась в том, что с ростом атомной массы химических элементов их свойства меняются не монотонно, а периодически. После определенного количества разных по свойствам элементов, расположенных по возрастанию атомного веса, свойства начинают повторяться. Отличием работы Менделеева от работ его предшественников было то, что основ для классификации элементов у Менделеева была не одна, а две - атомная масса и химическое сходство. Для того, чтобы периодичность полностью соблюдалась, Менделеев исправил атомные массы некоторых элементов, несколько элементов разместил в своей системе вопреки принятым в то время представлениям об их сходстве с другими, оставил в таблице пустые клетки, где должны были разместиться пока не открытые элементы.
В 1871 г. на основе этих работ Менделеев сформулировал Периодический закон, форма которого со временем была несколько усовершенствована.
Периодическая система элементов оказала большое влияние на последующее развитие химии. Она не только была первой естественной классификацией химических элементов, показавшей, что они образуют стройную систему и находятся в тесной связи друг с другом, но и явилась могучим орудием для дальнейших исследований. В то время, когда Менделеев на основе открытого им периодического закона составлял свою таблицу, многие элементы еще не были известны. В течение следующих 15 лет предсказания Менделеева блестяще подтвердились; все три ожидаемых элемента были открыты (Ga, Sc, Ge), что было величайшим триумфом периодического закона.
СТАТЬЯ «МЕНДЕЛЕЕВ»
Менделеев (Дмитрий Иванович) - проф., род. в Тобольске, 27 января 1834 г.). Отец его, Иван Павлович, директор тобольской гимназии, вскоре ослеп и умер. Менделеев, десятилетним мальчиком, остался на попечении своей матери, Марии Дмитриевны, урожденной Корнильевой, женщины выдающегося ума и пользовавшейся общим почетом в местном интеллигентном обществе. Детство и гимназические годы М. проходят в обстановке, благоприятной для образования самобытного и независимого характера: мать была сторонницей свободного пробуждения природного призвания. Любовь к чтению и изучению ясно выразилась в М. только по окончании гимназического курса, когда мать, решив направить своего сына к науке,вывезла его 15-летним мальчиком из Сибири сначала в Москву, а затем через год в Петербург, где и поместила в педагогический институт… В институте началось настоящее, всепоглощающее штудирование всех отраслей положительной науки… По окончании курса в институте, вследствие пошатнувшегося здоровья, уехал в Крым и был определен учителем гимназии, сначала в Симферополе, затем в Одессе. Но уже в 1856г. он опять вернулся в Петербург, поступил приват-доцентом в СПб. унив. и защитил диссертацию «Об удельных объемах», на степень магистра химии и физики… В 1859 г. М. был командирован за границу… В 1861 г. М. снова вступил приват-доцентом в Спб. университет. Вскоре затем опубликовал курс «Органической химии» и статью «О пределе СnН2n+ углеводородов». В 1863 г. М. был определен профессором CПб. технологического института и в течение нескольких лет много занимался вопросами техники: ездил на Кавказ для изучения нефти около Баку, производил сельскохозяйственные опыты Имп. Вольного экономического общества, издавал технические руководства и т. п. В 1865 г. производил исследования растворов спирта по их удельному весу, что послужило предметом докторской диссертации, которую и защищал в следующем году. Профессором СПб. унив. по кафедре химии М. был избран и определен в 1866 г. С тех пор научная его деятельность принимает такие размеры и разнообразие, что в кратком очерке можно указать только на важнейшие труды. В 1868 - 1870 гг. он пишет свои «Основы химии», где впервые проводится принцип его периодической системы элементов, давшей возможность предвидеть существование новых, еще неоткрытых элементов и с точностью предсказать свойства как их самих, так и их разнообразнейших соединений. В 1871 - 1875 гг. занимается исследованием упругости и расширения газов и публикует свое сочинение «Об упругости газов». В 1876 г. по поручению правительства едет в Пенсильванию для осмотра нефтяных американских месторождений и затем несколько раз на Кавказ для изучения экономических условий нефтяного производства и условий добычи нефти, повлекших за собой широкое развитие нефтяной промышленности в России; сам занимается исследованием нефтяных углеводородов, обо всем публикует несколько сочинений и в них разбирает вопрос о происхождении нефти. Приблизительно тогда же занимается вопросами, относящимися к воздухоплаванию и сопротивлению жидкостей, сопровождая свои изучения публикацией отдельных сочинений. В 80-х гг. он снова обращается к изучению растворов, результатом чего появилось соч. «Исследование водных растворов по удельному весу», выводы которого нашли столько последователей среди химиков всех стран. В 1887 г., во время полного солнечного затмения, поднимается один на аэростате в Клину, сам производит рискованную поправку клапанов, делает шар послушным и заносит в летописи этого явления все, что удалось заметить. В 1888 г. изучает на месте экономические условия Донецкой каменноугольной области. В 1890 г. М. прекратил чтение своего курса неорганической химии в СПб. университете. Другие обширные экономические и государственные задачи с этого времени начинают особенно занимать его. Назначенный членом совета торговли и мануфактур, принимает самое деятельное участие в выработке и систематическом проведении покровительственного для русской обрабатывающей промышленности тарифа и публикует сочинение «Толковый тариф 1890 г.», трактующее по всем статьям, почему для России наступила необходимость такого покровительства. Одновременно он привлекается военным и морским министерствами к вопросу о перевооружении русской армии и флота для выработки типа бездымного пороха и после командировки в Англию и Францию, которые тогда уже имели свой порох, назначается в1891 г. консультантом при управляющем морским министерством по пороховым вопросам и, работая вместе со служащими (своими бывшими учениками) в научно-технической лаборатории морского ведомства, открытой специально ради изучения означенного вопроса, уже в самом начале 1892 г. указывает требующийся тип бездымного пороха, названного пироколлодийным, универсального и легко приспособляемого ко всяким огнестрельным орудиям. С открытием в министерстве финансов палаты мер и весов, в 1893 г., определяется в ней ученым хранителем мер и весов и начинает издание «Временника», в котором публикуются все измерительные исследования, производимые в палате. Чуткий и отзывчивый ко всяким научным вопросам первостепенной важности, М. также живо интересовался и другими явлениями текущей общественной русской жизни, и везде, где возможно, сказал свое слово… С 1880 г. он начал интересоваться художественным миром, особенно русским, собирает художественные коллекции и т. п., а в 1894 г. избирается действительным членом Имп.академии художеств... Первостепенной важности разнообразные научные вопросы, бывшие предметом изучения М., по своей многочисленности не могут быть здесь перечислены. Он написал до 140 работ, статей и книг. Но время для оценки исторического значения этих трудов еще не наступило, и М., будем надеяться, еще долго не перестанет исследовать и высказывать свое мощное слово по вновь возникающим вопросам, как науки, так и жизни...
РУССКОЕ ХИМИЧЕСКОЕ ОБЩЕСТВО
Русское химическое общество - научная организация, основанная при Санкт-Петербургском университете в 1868 г. и представлявшая собой добровольное объединение российских химиков.
О необходимости создания Общества было заявлено на 1-м Съезде русских естествоиспытателей и врачей, состоявшемся в Санкт-Петербурге в конце декабря 1867 - начале января 1868 г. На Съезде было оглашено решение участников Химической секции:
«Химическая секция заявила единодушное желание соединиться в Химическое общество для общения уже сложившихся сил русских химиков. Секция полагает, что это общество будет иметь членов во всех городах России, и что его издание будет включать труды всех русских химиков, печатаемые на русском языке».
К этому времени уже были учреждены химические общества в нескольких европейских странах: Лондонское химическое общество (1841), Химическое общество Франции (1857), Немецкое химическое общество (1867); Американское химическое общество было основано в 1876 г.
Устав Русского химического общества, составленный в основном Д.И. Менделеевым, был утвержден Министерством народного просвещения 26 октября 1868 г., а первое заседание Общества состоялось 6 ноября 1868 г. Первоначально в его состав вошли 35 химиков из Петербурга, Казани, Москвы, Варшавы, Киева, Харькова и Одессы. В первый год своего существования РХО выросло с 35 до 60 членов и продолжало плавно расти в последующие годы (129 - в 1879 г., 237 - в 1889 г., 293 - в 1899 г., 364 - в 1909 г., 565 - в 1917 г.).
В 1869 г. у РХО появился собственный печатный орган - «Журнал Русского химического общества» (ЖРХО); журнал выходил 9 раз в год (ежемесячно, кроме летних месяцев).
В 1878 г. РХО объединилось с Русским физическим обществом (основано в 1872 г.) в Русское физико-химическое общество. Первыми Президентами РФХО были А.М. Бутлеров (в 1878-1882 гг.) и Д.И. Менделеев (в 1883-1887 гг.). В связи с объединением с 1879 г. (с 11-го тома) «Журнал Русского химического общества» был переименован в «Журнал Русского физико-химического общества». Периодичность издания составляла 10 номеров в год; журнал состоял из двух частей - химической (ЖРХО) и физической (ЖРФО).
На страницах ЖРХО впервые были напечатаны многие труды классиков русской химии. Можно особо отметить работы Д.И. Менделеева по созданию и развитию периодической системы элементов и А.М. Бутлерова, связанные с разработкой его теории строения органических соединений… За период с 1869 по 1930 г. в ЖРХО было опубликовано 5067 оригинальных химических исследований, печатались также рефераты и обзорные статьи по отдельным вопросам химии, переводы наиболее интересных работ из иностранных журналов.
РФХО стало учредителем Менделеевских съездов по общей и прикладной химии; три первых съезда прошли в С.-Петербурге в 1907, 1911 и 1922 гг. В 1919 г. издание ЖРФХО было приостановлено и возобновлено лишь в 1924 г.
Как пользоваться таблицей Менделеева? Для непосвященного человека читать таблицу Менделеева – всё равно, что для гнома смотреть на древние руны эльфов. А таблица Менделеева может рассказать о мире очень многое.
Помимо того, что сослужит вам службу на экзамене, она еще и просто незаменима при решении огромного количества химических и физических задач. Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Периодическая система химических элементов (таблица Менделеева) – это классификация химических элементов, которая устанавливает зависимость различных свойств элементов от заряда атомного ядра.
История создания Таблицы
Дмитрий Иванович Менделеев был не простым химиком, если кто-то так думает. Это был химик, физик, геолог, метролог, эколог, экономист, нефтяник, воздухоплаватель, приборостроитель и педагог. За свою жизнь ученый успел провести фундаментально много исследований в самых разных областях знаний. Например, широко распространено мнение, что именно Менделеев вычислил идеальную крепость водки – 40 градусов.
Не знаем, как Менделеев относился к водке, но точно известно, что его диссертация на тему «Рассуждение о соединении спирта с водой» не имела к водке никакого отношения и рассматривала концентрации спирта от 70 градусов. При всех заслугах ученого, открытие периодического закона химических элементов – одного их фундаментальных законов природы, принесло ему самую широкую известность.

Существует легенда, согласно которой периодическая система приснилась ученому, после чего ему осталось лишь доработать явившуюся идею. Но, если бы все было так просто.. Данная версия о создании таблицы Менделеева, по-видимому, не более чем легенда. На вопрос о том, как была открыта таблица, сам Дмитрий Иванович отвечал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово»
В середине девятнадцатого века попытки упорядочить известные химические элементы (известно было 63 элемента) параллельно предпринимались несколькими учеными. Например, в 1862 году Александр Эмиль Шанкуртуа разместил элементы вдоль винтовой линии и отметил циклическое повторение химических свойств.
Химик и музыкант Джон Александр Ньюлендс предложил свой вариант периодической таблицы в 1866 году. Интересен тот факт, что в расположении элементов ученый пытался обнаружить некую мистическую музыкальную гармонию. В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.

В 1869 году была опубликована первая схема таблицы, а день 1 марта 1869 года считается днем открытия периодического закона. Суть открытия Менделеева состояла в том, что свойства элементов с ростом атомной массы изменяются не монотонно, а периодически.
Первый вариант таблицы содержал всего 63 элемента, но Менделеев предпринял ряд очень нестандартных решений. Так, он догадался оставлять в таблице место для еще неоткрытых элементов, а также изменил атомные массы некоторых элементов. Принципиальная правильность закона, выведенного Менделеевым, подтвердилась очень скоро, после открытия галлия, скандия и германия, существование которых было предсказано ученым.
Современный вид таблицы Менделеева
Ниже приведем саму таблицу
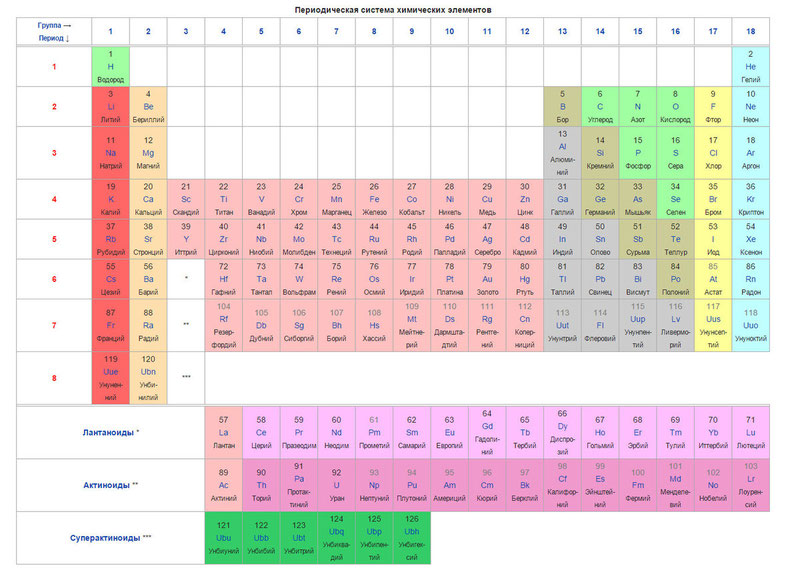
Сегодня для упорядочения элементов вместо атомного веса (атомной массы) используется понятие атомного числа (числа протонов в ядре). В таблице содержится 120 элементов, которые расположены слева направо в порядке возрастания атомного числа (числа протонов)
Столбцы таблицы представляют собой так называемые группы, а строки – периоды. В таблице 18 групп и 8 периодов.
- Металлические свойства элементов при движении вдоль периода слева направо уменьшаются, а в обратном направлении – увеличиваются.
- Размеры атомов при перемещении слева направо вдоль периодов уменьшаются.
- При движении сверху вниз по группе увеличиваются восстановительные металлические свойства.
- Окислительные и неметаллические свойства при движении вдоль периода слева направо увеличиваются.
Что мы узнаем об элементе по таблице? Для примера, возьмем третий элемент в таблице – литий, и рассмотрим его подробно.

Первым делом мы видим сам символ элемента и его название под ним. В верхнем левом углу находится атомный номер элемента, в порядке которого элемент расположен в таблице. Атомный номер, как уже было сказано, равен числу протонов в ядре. Число положительных протонов, как правило, равно числу отрицательных электронов в атоме (за исключением изотопов).
Атомная масса указана под атомным числом (в данном варианте таблицы). Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Вот и закончился наш курс "Таблица Менделеева для чайников". В завершение, предлагаем вам посмотреть тематическое видео, и надеемся, что вопрос о том, как пользоваться периодической таблицей Менделеева, стал вам более понятен. Напоминаем, что изучать новый предмет всегда эффективнее не одному, а при помощи опытного наставника. Именно поэтому, никогда не стоит забывать о студенческом сервисе , который с радостью поделится с вами своими знаниями и опытом.
В России скажут, что таблицу Менделеева изобрел, конечно, Менделеев. Приятно видеть в соотечественниках таких первооткрывателей и первопроходцев, как И.И.Ползунов, Д.И.Менделеев, А.С.Попов, К.Э.Циолковский, С.П.Королев, Ю.А.Гагарин. Однако, на Западе почему-то фигурируют другие имена...
Д.И.Менделеев опубликовал свою первую схему периодической таблицы в 1869 г. в статье "Соотношение свойств и атомных весов элементов", извещение об открытии было разослано в феврале 1869 г. Сам Д.И.Менделеев дал следующую формулировку:
"Свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса".
Таким образом, по мнению историков, в том числе, отечественных, сущность открытия Менделеева заключалась в том, что с ростом атомной массы химических элементов их свойства меняются не монотонно, а периодически. А также отличием работы Менделеева от работ его предшественников считают то, что основ для классификации элементов была не одна, а две - атомная масса и химическое свойство.
Однако, давайте посмотрим, как обстояло дело с сущностью у предшественников.
Немецкий химик И.В.Дёберейнер (1780-1849) впервые установил закономерности изменения свойств элементов в зависимости от возрастания атомных весов: атомный вес среднего элемента в триаде равен среднему арифметическому атомных весов первого и третьего элементов триады. Первая такая закономерность была обнаружена им в 1817 г. для кальция, стронция и бария, позже - для других триад. Но это и есть периодическое повторение свойств химических элементов в зависимости от их атомного веса, т.е. формально все то, что есть у Д.И.Менделеева.

Официально Дёберейнер опубликовал свой "закон триад" в 1829 г. Другое дело, что триад, как и самих известных элементов, было тогда маловато, поэтому историки осторожно формулируют так: закон триад Дёберейнера подготовил почву для систематизации элементов, завершившейся созданием периодического закона. Что ж, почва - это тоже немало!
Вот таблица Дёберейнера.

Не густо. Если бы было бы известно в те времена больше элементов и их атомных весов, то Дёберейнер, несомненно, догадался бы о большем.
Французский геолог и химик А.Э.Шанкуртуа (1820-1886) в 1862 г. предложил систематизацию, основанную на закономерном изменении атомных масс. Он отметил элементы точками на поверхности цилиндра. Элементы, атомные веса которых отличались на 16 или на кратное 16, располагались на одной вертикали, на которой шло и совпадение других свойств. Работа осталась незамеченной, о ней вспомнили только после открытия Д.И.Менделеевым Периодического закона. Винтовой график на цилиндре точнее отражает последовательность свойств, а на плоской таблице Менделеева единая линия рвется.

Вот еще впечатляющая периодическая система Шанкуртуа в виде спирали.

Английский химик Д.А.Ньюлендерс (1837-1898) составил таблицу, в которой расположил все известные химические элементы в порядке увеличения их атомных весов. В статье от 20 августа 1864 г. впервые в истории им была прямо высказана идея о периодичности изменения свойств химических элементов. Хотя предшественники Ньюлендерса не упирали на периодичность, но возможно, лишь потому, что она и так была очевидна в их схемах.

18 августа 1865 г. Ньюлендерс опубликовал новую таблицу химических элементов, назвав ее "законом октав". 1 марта 1866 г. Ньюлендерс сделал доклад "Закон октав и причины химических отношений среди атомных весов" на заседании Лондонского химического общества. К сожалению, доклад не вызвал интереса, так как и без Ньюлендерса было много попыток поиска закономерностей среди атомных весов элементов.

Немецкий химик Ю.Л.Мейер (1830-1895) В 1864 г. опубликовал таблицу из 28 элементов, размещенных в 6 столбцов согласно их валентности. Хотя валентность и атомная масса - разные вещи, но из-за их связи таблица все равно получилась по весам, причем в таблице прямо указаны массы.

В декабре 1869 г. Мейер написал и в 1870 г. опубликовал работу "Природа элементов как функция их атомного веса". Таблица Мейера 1870 г. в некоторых отношениях совершеннее первого варианта таблицы Менделеева, но существенно, что дата на год позже.

В те времена отсутствовал не только Интернет, но телевидение и радио. Обмен информацией происходил не быстро. Даже в наше время ученые часто не знают об открытиях коллег и делают их независимо. Анекдотичен случай с великим К.Э.Циолковским и его кинетической теорией газов, на которую тот же Д.И.Менделеев написал Циолковскому убийственный ответ: кинетическая теория газов открыта 25 лет назад.

Во всяком случае, Лондонское королевское общество признало равные права и в 1882 г. присудило золотые медали Менделееву и Мейеру "за открытие периодических соотношений атомных весов". С такой формулировкой вполне можно было наградить еще десяток человек.
Поэтому весьма странно категорическое заявление Д.И.Менделеева: "г.Майер раньше меня не имел периодического закона, а после меня ничего нового к нему не добавил". Вот так! Ничем делиться не собираюсь.
А при указанной формулировке делиться с Мейером нечем. Из формально заявленной сущности открытия Д.И.Менделееву не принадлежит ровно ничего. Задолго до него и до Мейера десяток известных химиков и, наверное, тысячи энтузиастов классифицировали химические элементы согласно их свойствам и по возрастанию атомного веса, кто-то более успешно, кто-то - менее. Новизна работы Д.И.Менделеева оказалась никак не выделена.
Более того, в начале XX века с открытием строения атома было установлено, что периодичность изменения свойств химических элементов определяется не атомным весом, а зарядом ядра. Таким образом был поставлен жирный крест на атомном весе, который, как выяснилось, зависит еще от количества нейтронов и потому никак не может быть определяющим.
Что же тогда получается? Вообще, не было никакого открытия? А были сплошные заблуждения, которые постепенно рассеивались огромным множеством исследователей? Может быть, и так. На истории химии прекрасно видно, как фактический материал от тех, кто колдует с пробирками, постепенно приводит к новым выводам, теоретики в некотором роде выполняют волю этого материала.
Если кто-то сделал новый небольшой вывод, то это не значит, что он гениальнее предшественников. Просто пришло время очередного вывода...
И все же есть во всей этой истории с таблицей Менделеева поворотный момент, которым вправе гордиться Д.И.Менделеев и вся Россия. Его скромно называют особенностью таблицы Менделеева, но, по-моему, в этом самая великая суть: Менделеев оставил дырки в своей таблице! Вот в чем главная заслуга Менделеева, а не в том, о чем заявил сам Д.И.Менделеев и чего вдоволь было у его предшественников.
Много ли пользы от дырок? Смотря каких! Благодаря этим дыркам, таблица Д.И.Менделеева превратилась в мощнейший инструмент научного поиска и развития всей химической науки. Теперь стало ясно, где и что надо искать! Поэтому за дырки надо было медали давать! Правда, еще надо поискать смельчаков, которые решились бы публично восхвалять пустое место.
Впрочем, стало ясно не сразу. Поначалу Д.И.Менделеев не придавал большого значения своей таблице. В ту пору только не ленивый не переставлял подобно ребенку кубики с названиями химических элементов. Для серьезного ученого это было более чем сомнительным занятием.
Нельзя сказать, что порядок среди элементов не нужен. Но одно дело работать с колбами, у станка или в поле, и совсем другое - конторские подсчеты, несулящие никакой пользы.
Это мы сейчас знаем, что дырки Менделеева были гениальными. А сначала они были неуместным аппендиксом, прямым признанием несостоятельности таблицы. Придумывать всякие фантастические материи и пространства, чтобы залатать прорехи в какой-нибудь свежеиспеченной теории, - это плохой тон для серьезной практической науки.
Благодаря своим дыркам, Д.И.Менделеев предсказал обнаружение ряда неизвестных тогда химических элементов, но мало ли вообще на свете предсказателей! Конец света без устали предсказывают, а это поважнее, чем как-то элемент, встречающийся в микроскопических дозах.
Предсказанные элементы могли не найтись. Собственно, никаких доказательств у Д.И.Менделеева не было. И что тогда? Забыли бы, как массу иных предсказаний. Например, считали, что между орбитами Марса и Юпитера некогда существовала планета Фаэтон, но сейчас уверяют, что ее там никогда не было. Считали, что есть теплород, но тоже не оказалось.
Тогда с какой стати должны найтись промежуточные элементы? Мало ли что там задумали Бог или матушка-природа! Нет, и все! И можно жаловаться хоть в спортлото.
Но нашлись промежуточные элементы! Не сразу, но нашлись. Через шесть лет в 1875 г. обнаружили предсказанный галлий, а в 1879 г. скандий. Одну находку можно было счесть случайной. Но после второго сюрприза скептическая научная общественность запела совсем другим голосом и аж на золотые медали расщедрилась. Действительно, не часто предсказания сбываются.
В 1885 г. был открыт предсказанный германий, а дальше пошло-поехало.
Тут уж Д.И.Менделеев осмелел! В споре за первенство с Мейером, наш соотечественник прямо, доходчиво и без признаков скромности заявил:
"По праву творцом научной идеи должно того считать, кто понял не только философскую, но и практическую сторону дела, сумел так его поставить, что в новой истине все могли убедиться и она стала всеобщим достоянием".
Вот так! Дело, оказывается, не в периодичности, а в практической стороне дела.
Правда, сам Дмитрий Иванович "понял" это далеко не сразу, а гораздо позже, когда больше другие "сумели поставить" "практическую сторону дела". Но это уже не так важно. Главное, что путь к "всеобщему достоянию" был открыт. И лежал этот путь через дырки. Наверное, никогда не было в истории и уже не будет таких величайших и плодотворнейших дырок!
